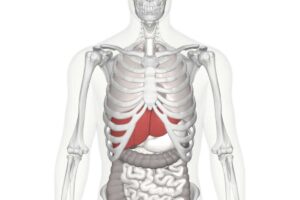
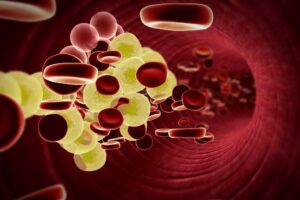
أمراض الدم الخطيرة تحدث نتيجة اضطراب في مكونات الدم، باعتبار الدم هو نسيج حي يتكون من السوائل والمواد الصلبة، يحتوي الجزء السائل المسمى البلازما على الماء والأملاح المعدنية والبروتينات، أما الجزء الصلب يحتوي على خلايا الدم الحمراء والبيضاء والصفائح الدموية.
تؤثر أمراض واضطرابات الدم على جزء أو أكثر من أجزاء الدم وتمنع الدم من القيام بعمله. وتسبب العديد من الأمراض واضطرابات الدم بسبب الجينات، تشمل الأمراض الأخرى، والآثار الجانبية للأدوية وعدم وجود بعض العناصر الغذائية في النظام الغذائي، ومن أمراض الدم الخطيرة التي قدمت معلومات عنها مؤسسةMDS الدولية ثلاثة أمراض نادرة في نخاع العظم هي: فقر الدم اللاتنسجي Aplastic Foundation ومتلازمات خلل التنسج النخاع (MDS) والبيلة الخضابية الانتيابية الليلية Paroxysmal Nocturnal.
فقر الدم اللاتنسجي ( Aplastic Anemia)
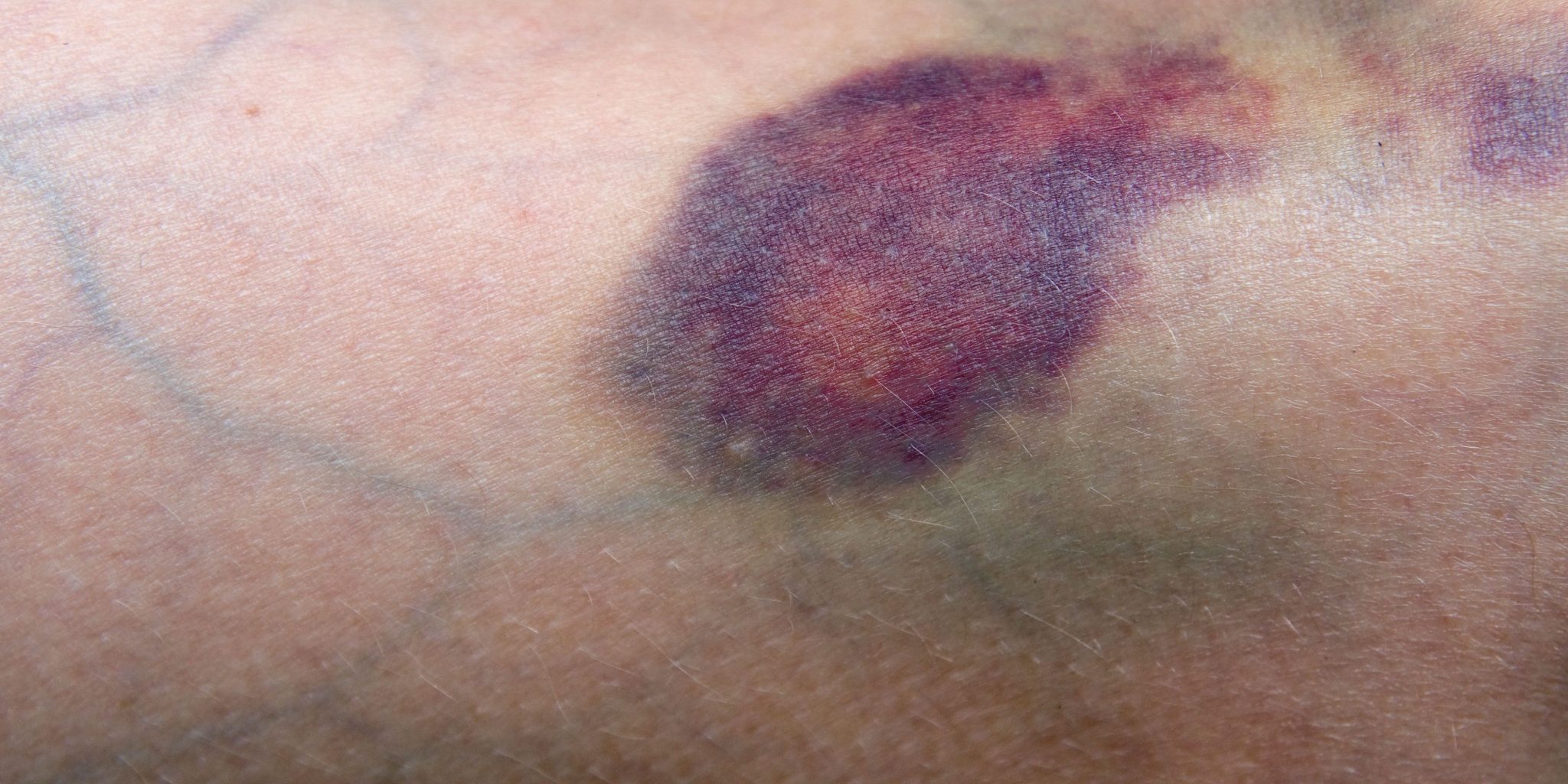
مرض يصيب نخاع العظم، يحدث عندما يتوقف النخاع العظمي عن إنتاج ما يكفي من خلايا الدم الحمراء وخلايا الدم البيضاء والصفائح الدموية للجسم، حيث إن خلايا الدم التي ينتجها النخاع طبيعية، لكنها غير كافية. فيمكن أن يكون فقر الدم اللاتنسجي معتدلًا أو شديدًا أو شديد الخطورة. بالإضافة إلى أن الأشخاص الذين يعانون من فقر الدم اللاتنسجي الشديد معرضون لخطر الإصابة بنزيف أو عدوى تهدد حياتهم.
أسباب الإصابة بهذا المرض:
من المعروف أن العديد من العوامل تؤدي إلى فقر الدم اللاتنسجي، على الرغم من ذلك لم تعرف الآلية بشكل دقيق حتى هذا الوقت، ربما تكون خلل في المناعة الذاتية لدى المرضى.
فقر الدم اللاتنسجي، المتكرر نسبيًا، قد يكون ثانويًا وسببه:
- مناعي.
- خلل في نظام النخاع، ربما جيني.
- التناسب بين تأثير السمية النخاعية والجرعة، وتناسب التأثير مع مدة التعرض.
- الإشعاعات المؤينة (النظائر، المتفجرات النووية).
- فقر الدم اللاتنسجي يتطور أحيانًا مع تأخير كبير في التعرض للأشعة غالبًا ما يرتبط بمجموعة معقدة.
- الإصابة بمرض الهزال: والذي تكون أعراضه تساقط الشعر، الإسهال المزمن، ويمكن أن يتحول بسهولة إلى سرطان الدم الحاد.
- الأدوية المستخدمة في علاج السرطان: خردل النيتروجين، يوريتان، أميثوبترين، 6 ميركابتوبورين، المايلان.. إلخ.
- فقر الدم اللاتنسجي هو أحد مضاعفات علاج الأمراض الخبيثة (سرطان الدم، السرطانات) بواسطة الأدوية.
- البنزين ومشتقاته، يستخدم البنزين (أو البنزول) كمذيب عضوي في الصناعة الكيميائية، كمادة مضافة إلى بنزين السيارة وكمزيل شحوم للأجزاء الميكانيكية. يمكن أن تكون مسؤولة عن الملوثات.
- الفيناسيتين كان دواء غير موصوف يستخدم كمسكن، وقد تم سحبه من السوق بسبب آثاره الجانبية (الفشل الكلوي وفقر الدم اللاتنسجي) في الاتحاد الأوروبي.
يوصف فقر الدم اللاتنسجي مع العديد من الأمراض الوراثية: فقر الدم Fanconi، خلل التقرن الخلقي. هذه الأسباب نادرة ويعتبر 5% فقط من فقر الدم اللاتنسجي بسبب العوامل الوراثية، وفي بعض الأحيان لا يتم تحديد سبب فقر الدم اللاتنسجي.
علاج فقر الدم اللاتنسجي (البدائي):
إن السبب الدقيق غير معروف، لكن العلاج المحتمل هو زرع نخاع العظم.
أعراض المرض وتطوره:
في البداية يظهر على الشخص المصاب التعب والشحوب (زيادة فقر الدم). وتزداد خطورة الإصابات (التهاب اللثة، التهاب اللوزتين، التهابات الجهاز التنفسي، تعفن الدم) والنزيف (اللثة، رعاف، نزف الدم، نزيف دماغي) وفي هذه المرحلة الأخيرة تشكل متلازمة تسمى سرطان الدم فرانك. ولكن تطور هذا المرض لا يمكن التنبؤ به ولكن معدل الوفيات يتجاوز 50 ٪.
من الأفضل معرفة الحالات التي تكون مسبباتها معروفة، حيث يكون من الممكن إيقاف التعرض للعامل المسبب. وفي أغلب الأحيان يمكن التمييز بين الحالات الحادة، التحول إلى سرطان الدم الحاد التي عادة ما تكون قاتلة في أقل من عام، والأشكال المزمنة التي تقل فيها معدلات الوفيات.
تشخيص المرض:
يتم تشخيص الإصابة عن طريق عملية الهيموغرام، ويتجلى الطابع اللاتنسجي لفقر الدم من خلال فحص النخاع فتظهر خلايا النخاع الفقيرة. ويمكن إجراء خزعة من نخاع العظم لفهم الخصائص بشكل أفضل.
علاج مرض اللاتنسجتي:
يعتبر القضاء على العامل المسبب أي عدم التعرض للإشعاعات المؤينة أو العامل السام، علاج جيد لكن هذا العلاج غير فعال بشكل جذري.
العلاج البديل:
نقل الدم وهو ضروري في الحالات الشديدة، ولكن يجب تباعد عمليات نقل الدم إلى أقصى حد ممكن، عمليات نقل الدم المتكررة، لها عدد من العيوب الطبية بالإضافة إلى تكلفتها.
وقد يصبح من المستحيل إيقاف هذا العلاج البديل بمجرد البدء به، ومن الضروري زيادة وتيرة عمليات نقل الدم بسرعة. لأن لذلك تأثير مثبط على الكريات الحمراء الناقصة بالفعل، عن طريق إزالة التحفيز من النخاع وبالنتيجة نقص الأكسجة.
لكن هناك خطر تراكمي للانتقال الفيروسي
يتوقع أن يؤدي عدد معين من عمليات نقل الدم إلى التطعيم ضد مستضدات بعض خلايا الدم المانحة وكذلك ضد بعض بروتينات المصل (خاصة الغلوبولين المناعي والبروتينات الدهنية منخفضة الكثافة التي هي من تعدد الأشكال الوراثية المعقدة)، وبالتالي خطر وقوع حوادث نقل الدم.
متلازمات خلل التنسج النقوي (MDS)
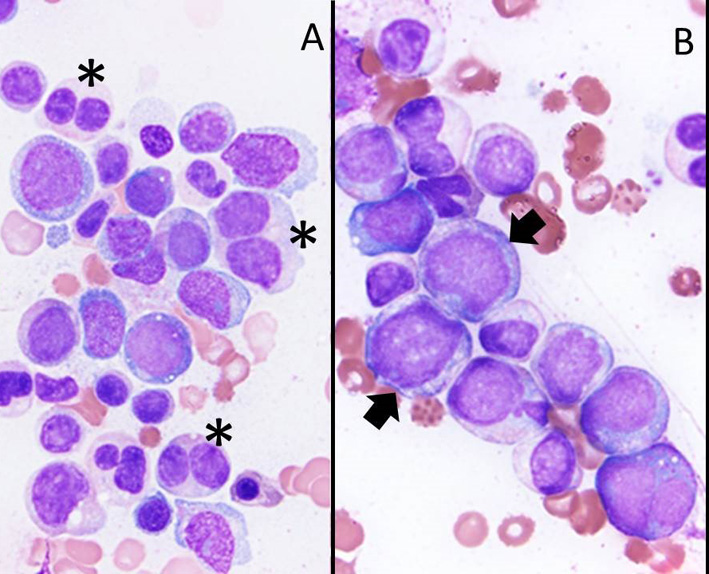
هي اضطرابات في النخاع العظمي، والتي تسمى منذ فترة طويلة فقر الدم الحراري، هي اعتلال مخاطي نسيلي (مما يعني أنها جميعًا مستمدة من نفس السلائف المكونة للدم). فإن المرضى الذين يعانون من هذه الأمراض، تفشل الخلايا الجذعية المكونة للدم الموجودة في نخاع العظام في إنتاج خلايا دم صحية كافية. هذا هو السبب في أن هؤلاء الأشخاص قد يفتقرون إلى خلايا الدم الحمراء، أو خلايا الدم البيضاء أو الصفائح الدموية (الخلايا الصغيرة التي تساعد في تخثر الدم). بالإضافة إلى ذلك، ينتج النخاع العظمي خلايا غير طبيعية تسمى خلل التنسج النخاعي. الذي يسود عند كبار السن مع غالبية البشر، الذين يبلغ متوسط أعمارهم عند التشخيص حوالي 70 عامًا. وقد تحدث 8 إلى 10٪ من الحالات تحت سن 50 عامًا.
لا يزال أصل هذه الأمراض غير معروف، وربما يكون في بعض الأحيان وراثيًا (خلقي) أو بسبب طفرة جينية مكتسبة أو العوامل السمية (التعرض للبنزين، العلاج الكيميائي أو العلاج الإشعاعي) أو ممكن بسبب العوامل البيئية.
التصنيف و المفردات حسب الفرنسية الأمريكية البريطانية FAB
تم استخدام المصطلحات التاريخية عن حالة سرطان الدم، وقد أدت أهمية التصنيف المشترك إلى قيام فرنسا والولايات المتحدة والمملكة المتحدة في عام 1976م، بتصنيف الفرنسية الأمريكية البريطانية أو FAB، من سرطان الدم الحاد.
وهو يصف نوعين من الـ SMD:
- فقر الدم الحر مع الانحلال المفرط (AREB).
- سرطان الدم النخاعي المزمن (LMMC).
يتم استخدام تصنيف FAB المنشور في عام 1982م، لجميع MDS، ولكن تم إصدار مقترحات جديدة مؤخرًا لتصنيف أمراض الأورام الخبيثة تحت رعاية منظمة الصحة العالمية.
يحدد تصنيف FAB (الفرنسي الأمريكي البريطاني) لمتلازمات خلل التنسج النخاعي لعام 1982م، خمس فئات تشخيصية:
- فقر الدم الحراري (AR).
- فقر الدم الأرومي مجهول السبب (آسيا).
- فقر الدم الحر مع زيادة التحلل (AREB).
- فقر الدم الناجم عن التحلل الزائد في التحول (AREB-t).
- سرطان الدم النخاعي المزمن (LMMC).
في هذا التصنيف، فإن وجود تشوهات المورفولوجية (Dysmyelopoiesis) يجعل من الممكن تشخيص MDS.
تصنيف منظمة الصحة العالمية:
يحدد تصنيف منظمة الصحة العالمية الجديد لخلل التنسج النخاع ستة فئات مختلفة عن تصنيف FAB:
- قلة الخلايا الحرارية مع خلل التنسج الأحادي.
- فقر الدم الحر ARمع أو بدون الأرومة ARS.
- قلة الكريات الحرارية أو متلازمة خلل التنسج النخاعي مع خلل التنسج النخاعي المتعدد (CRMD).
- فقر الدم الحر مع زيادة التحلل (AREB).
- متلازمات خلل التنسج النقوي غير القابلة للتصنيف.
- الفيزيولوجيا المرضية.
تشخيص متلازمات خلل التنسج النقوي(MDS):
- تظهر الآثار المترتبة على قلة الكريات الحمر: متلازمة نقص الصفيحات الدموية، النزيف، العدوى الوخيمة والمتكررة العدلات (هو اضطراب في الدم يتميز بانخفاض غير طبيعي لنوع من خلايا الدم البيضاء)، ومتلازمة فقر الدم.
- في حالات نادرة، يلاحظ تضخم الطحال المعتدل، المتعلق بسرطان الدم النخاعي المزمن (CMML)، مجموعة متنوعة من متلازمة خلل التنسج النخاعي.
- ارتباط السيتوبينات، من حيث العدد والأهمية المتغيرة، هو الذي يوجه التشخيص: فقر الدم الكلي Artegenerative.
- نقص الكريات البيض مع قلة العدلات يصاحبها في بعض الأحيان كريات الوحيدات في حالة LMMC.
يتيح التصنيف الفرنسي الأمريكي البريطاني (FAB) استنادًا إلى النسبة المئوية لانحلال الدم ونخاع العظام، ونسبة الأرومة الحبيبية في النخاع الشوكي وحيدات الدم، إمكانية التمييز بين أنواع مختلفة من متلازمة خلل التنسج النخاعي. لم يعد يتم استخدام تصنيف FAB لتصنيف متلازمات خلل التنسج المختلفة، وقد تم استبدالها بتصنيف منظمة الصحة العالمية.
الاستنتاج بعد دراسة المرض:
متلازمات خلل التنسج النخاعي شائعة عند كبار السن وهي أكثر الحالات التي تسبق الإصابة بسرطان الدم شيوعًا. تشخيصهم وتصنيفهم بسيط. لا يمكن إلا الأمل في الشفاء التام، وكلما كان الشخص أصغر سنًا، زادت فرص النجاح. بعد سن الأربعين، فإن خطر الوفاة من خلال رفض الكسب غير المشروع يجعل الاستفادة من العلاج الكيميائي مفيدة من خلال عامل فرط الإيثيل الذي يثبته المرض.
حتى لو لم يعالج المرض، فإنه يستقر ويحقق 50 ٪ بقاء متوسط لمدة عامين مع نوعية جيدة من الحياة بالنسبة للمرضى. لهذا تحتاج إلى تقييم عام جيد للمريض واحترام الاستخدام الصحيح للدواء المحدد في دراسة GFM Aza 001. قبل هذا العلاج، كان 25 ٪ فقط لا يزالون على قيد الحياة بعد عامين أي أقل مرتين. يكمن الأمل في الجمع بين العلاج بعامل فرط الإيثيل مع علاج آخر وفي تقييم أكثر دقة للمريض والتشخيص، والذي ما زال يسمح بإبقاء المرضى لمدة أشهر أو حتى سنوات على قيد الحياة.
البيلة الهيموغلوبينية الانتيابية الليلية (PNH)
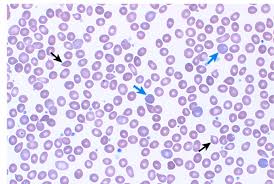
وهو مرض نادر وخطير يصيب الدم، فإن المرضى الذين يعانون من PNH تنهار خلايا الدم الحمراء لديهم، أي يزيد انحلال الدم. تحتوي خلايا الدم على بروتين يحميها من الجهاز المناعي، يحدث انحلال الدم عند غياب هذا البروتين. عندما يكتشفون أن لديهم مرض نادر في نخاع العظام.
الـ PNH هو مرض تم تحديده قبل وقت قصير من الحرب العالمية الثانية حتى الآن، تم تشخيص حوالي 500 حالة في فرنسا.
الفيزيولوجيا المرضية:
يحدث هذا الشرط بسبب طفرة في جين PIG-A المسؤول عن إنتاج الفوسفاتيديل-إينوسيتول غليكان PIG . PIG (ومشتقاته GPI) ضروري بحد ذاته لترسيخ الغشاء لعدة بروتينات في خلايا الدم، ولا سيما (CD 59، Decay Accelerating Factor (DAF هما بروتينان سطحيان لخلايا الدم الحمراء وحيدات الخلايا التي تمنع تكوين مجمع هجوم الغشاء المكمل. وبالتالي نقص حماية غشاء خلايا الدم الحمراء من التحلل بواسطة التكملة، المكمل أكثر نشاطًا في الوسط الحمضي، لذلك في النصف الثاني من الليل (درجة الحموضة في الدم أقل)، يحدث انحلال الدم (تحلل خلايا الدم الحمراء) بشكل أكبر خلال الليل.
بدايات معرفة هذا المرض:
في نهاية القرن التاسع عشر، وصف جول وستروبنغ حالة المرضى الذين يعانون من بيلة دموية متقطعة وانحلال الدم داخل الأوعية، وقد أسس الصورة السريرية الكلاسيكية للمرض مارشيافافا ونزاري عام 1911م، ثم ميشيل في عام 1931م.
يعتبر مرض الهيموغلوبين في الدم الليلي الانتيابي (PNH)، أو مرض مارشيافافا وميشيلي، من أمراض الخلايا الجذعية المكونة للدم. منذ بداية الثمانينات، أدى التقدم في قياس التدفق الخلوي ومؤخرًا في البيولوجيا الجزيئية إلى تقدم حقيقي في معرفة الفيزيولوجيا المرضية لهذا المرض النادر. ومن الأوصاف الأولى للمرض تم اعتبار الحساسية غير الطبيعية لخلايا الدم الحمراء تجاه الفعل التكميلي للمكملات (بروتينات الجهاز المناعي) كميزة رئيسية للمرض.
الأعراض:
هو فقر الدم الانحلالي يصيب البالغين، وتبدأ الأعراض بظهور البول الداكن في الصباح واليرقان المعتدل في بعض الأحيان. ويرافق ذلك ألم قطني ويواجه الكلى وقد يكون شديدًا، لا سيما في وقت مبكر من اليوم. ويصاحب فقر الدم علامة على تجديد معتدل وغالبًا ما تكون هناك درجة معينة من فشل النخاع العظمي.
وبالطبع، هناك كل العلامات الكلاسيكية لفقر الدم المزمن، عادة ما يتم التشخيص بعد بضعة أشهر فقط ومن الأعراض: تعب وضعف العضلات وضيق في التنفس عند القيام بأدنى جهد وشحوب الجلد وصداع.
تطور المرض:
هناك مخاطر التحول إلى سرطان الدم الحاد بعد بضع سنوات. قد يحدث أيضًا تثبيط نخاع العظم أي انسداد دموي في نخاع العظم، وهي آلية غير معروفة، ولكن ربما يتعلق بانحلال الدم داخل النخاع المصاحب لانحلال الدم، خلايا المكونة للدم تحمل أيضًا CD 55 و CD 59. قد يكون هناك مغفلات عفوية طويلة.
علاج الأعراض:
يجعل ندرة هذا المرض من الصعب تقييم فوائد العلاجات المستخدمة. في حالة فقر الدم الشديد أو الذي لا يمكن تحمله بشكل جيد، تظل التركيزات الكروية ضرورية بصرف النظر عن عمليات نقل الدم، قد يستفيد بعض المرضى من مكملات الحديد للتعويض عن فقدان البول اليومي من 20 ملغ من الحديد في شكل هيموسيديرين. لكن أخذ الحديد يمكن أن يسبب آلام في البطن.
من المعتاد أيضًا تكملة حمض الفوليك (فيتامين ب 9) لجميع المرضى الذين يعانون من فقر الدم الانحلالي المزمن نتيجة لإنتاج نخاع العظام التعويضي. يمكن وصف GCSF بأشكال مرنة، مع نتائج مختلطة. كما أن الإريثروبويتين (EPO)، يمكن أن يساعد في الحد من عمليات نقل الدم.
مثبطات المناعة. في الواقع تم استخدام السيكلوسبورين ومصل مضاد اللمفاويات بنجاح في بعض الأشكال شديدة النقص (تعداد دم منخفض).
اقرأ أيضًا: زراعة النخاع العظمي لمرضى سرطان الدم.